Kürzlich hat die chinesische staatliche Lebensmittel- und Arzneimittelbehörde (SFDA) offiziell den Zulassungsantrag für Tafolecimab (monoklonaler PCSK-9-Antikörper, hergestellt von INNOVENT BIOLOGICS, INC), INC, zur Behandlung von primärer Hypercholesterinämie (einschließlich heterozygoter familiärer Hypercholesterinämie und nicht-familiärer Hypercholesterinämie) angenommen Hypercholesterinämie) und gemischte Dyslipidämie.Dies ist der erste selbst hergestellte PCSK-9-Hemmer, der für die Vermarktung in China beantragt wurde.
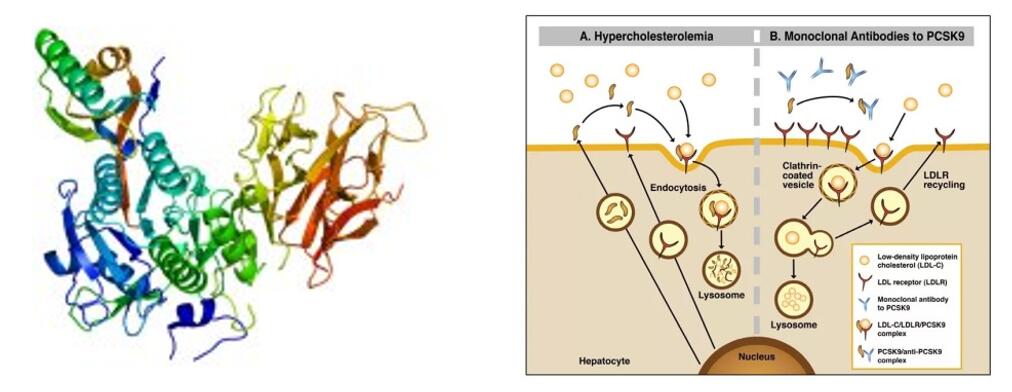
Tafolecimab ist ein innovatives biologisches Medikament, das von INNOVENT BIOLOGICS, INC. unabhängig entwickelt wurde. Der humane monoklonale IgG2-Antikörper bindet spezifisch an PCSK-9, um die LDLR-Spiegel zu erhöhen, indem die PCSK-9-vermittelte Endozytose reduziert wird, wodurch die LDL-C-Eliminierung erhöht und die LDL-C-Spiegel gesenkt werden.
In den letzten Jahren hat die Prävalenz von Dyslipidämie in China deutlich zugenommen.Die Prävalenz von Dyslipidämie und Hypercholesterinämie bei Erwachsenen liegt bei 40,4 % bzw. 26,3 %.Laut dem Bericht 2020 über kardiovaskuläre Gesundheit und Krankheiten in China befinden sich die Behandlungs- und Kontrollrate von Dyslipidämie bei Erwachsenen immer noch auf einem niedrigen Niveau, und die LDL-C-Compliance-Rate von Dyslipidämie-Patienten ist noch weniger zufriedenstellend.
Früher waren Statine die Hauptbehandlung für Hypercholesterinämie in China, aber viele Patienten erreichten das Behandlungsziel der LDL-C-Senkung nach der Behandlung immer noch nicht.Die Vermarktung von PCSK-9 hat den Patienten eine bessere Wirksamkeit gebracht.
Die Einreichung von Tafolecimab von INNOVENT BIOLOGICS, INC basiert auf den Ergebnissen von drei klinischen Studien, die in einer demokratischen Phase registriert wurden. Es hat ein gutes allgemeines Sicherheitsprofil, ähnlich den Sicherheitsmerkmalen von vermarkteten Produkten, und hat lange Intervalle erreicht (alle 6 Wochen). der Verwaltung.Die Ergebnisse der CREDIT-2-Studie wurden von der Jahrestagung 2022 des American College of Cardiology (ACC) als Abstract angenommen und online veröffentlicht.
Wenn der Antrag genehmigt wird, wird er die Blockade von PCSK-9 durchbrechen, China wird das vierte Land sein, das PCSK-9 nach den Vereinigten Staaten (Amgen), Frankreich (Sanofi) und der Schweiz (Novartis) hat.
Postzeit: 04.07.2022